周末的时候,有位朋友来访,在我这小办公室里面坐着聊聊天。
朋友经营着一个很小的IVD工厂,手上也有几个产品获得了注册证,一年也能有个五六百万的营销额。
聊着聊着,自然也就谈到了现在的热点,居家自测。
做为老板,最重要的工作之一就是寻找发展的方向,所以他一直很关注这方面。
我哈哈哈大笑说道,与其坐而论道,不如躬身入局,为何不把你手上那几个胶体金产品,拿去卖一卖,了解一下实际情况如何呢?
朋友有些吃惊,说,这样可以么,我这几个产品,既没有OTC标,预期用途里也没有写自测,就能够直接做To C生意,卖给消费者了么?
当然可以。要不要OTC标?
OTC这个概念,对于我们IVD人来说,是有点陌生的,因为它主要用在药品当中。
OTC是“Over-The-Counter”的缩写,指的是非处方药,这类药品不需医生的处方,消费者可以直接在药店、超市等地方购买使用。
在国内,OTC药品根据其安全性被分为甲类和乙类,分别用红标和绿标来标识。
甲类OTC,即红标OTC,通常在临床使用时间相对较短,安全性略低,因此用红色警示。这类药品虽属非处方药,但需要在执业药师的指导下购买和使用。
乙类OTC,即绿标OTC,其安全性相对更高,临床使用时间更长,经验更多。乙类OTC除了在药店出售,还可以在获得批准的超市、宾馆等地方销售。
在国内,只有药品才有OTC标志,器械一般是没有的。
当然,也不是没有特例,如果是药械组合的话,那么就有可能会有OTC标志。
例如,创口贴一般是一类医疗器械,是没有OTC标志的,但是含有消炎止痛药的创可贴,就属于药械组合,在这种情况下,很有可能就有OTC标志。
那么,在国际上面,有没有国家将医疗器械也分为OTC和非OTC呢?
有,美国。
在美国,OTC医疗器械是指可以直接向消费者销售而不需要医生处方的医疗设备。这些设备通常具有较低的风险,并且消费者能够根据产品标签的说明自行使用,比如创可贴、卫生棉条和避孕套等。
而非OTC医疗器械指的是那些需要医生处方才能购买和使用的医疗器械,它们通常具有较高的风险性,并且需要更严格的监管措施来确保其安全性和有效性。
之前,在有的研报当中,说诺辉的常卫清和Cologuard相比,优势是不需要医生开单就能直接使用,所以很容易起量,这就有点关公战秦琼的味道。
这主要是中美两家的政策不同,而这种不同的政策会塑造不同的市场风格,而用一个市场的情况去预测另一个完全不同的市场,正确率恐怕也不高。
好,现在我们可以回答第一个问题,消费者自用医疗器械,不需要OTC标志。预期用途中要不要写自测?
于是,让我们进入第二个问题。
是不是需要在预期用途当中,包含自用/自测的字样,才能直接销售给消费者呢?
答案是当前,不需要。
国内在这方面只有一点模糊的规定,在2017年颁布的《医疗器械网络销售监督管理办法》第十三条中,是这么规定的:
医疗器械零售企业从事医疗器械网络销售,应当销售给消费者。销售给消费者个人的医疗器械,应当是可以由消费者个人自行使用的,其说明书应当符合医疗器械说明书和标签管理相关规定,标注安全使用的特别说明。
问题在于,什么是可以由消费者个人自行使用的?是在预期用途当中必须规定嘛?
我给大家举个例子。
创可贴是大家在药店非常容易买到的医疗器械,我也买了一盒,然后拍下了它的说明书,如下图所示,

从图中,我们可以看到,在这一类器械的说明书当中,实际上并没有特别标明消费者个人自行使用的相关字样。
当然,创可贴可能和IVD产品相差是比较远的,我们看一个更合适的例子——早早孕试剂。
早早孕试剂就是HCG检测试剂,用于妊娠早期的辅助诊断,我们在药店和超市里面,都能买到相应的产品,我在网上找到一份说明书,如下图所示,

从图中,也可以看到,说明书并没有特别标明消费者个人自行使用的相关字样。
在2017年,NMPA在其网站上发表了《购买家用医疗器械需要注意什么?》的问答,其中对于产品资质的规定如下所示,
查看产品资质。医疗器械产品应具备《医疗器械产品注册证》(或备案凭证),《医疗器械生产许可证》(或备案凭证)。有一些普通商品宣传治疗功效混淆视听,如增高仪、减肥仪等,日常健身的健身器材以及一些含保健功能的衣服、帽子、鞋、袜、手镯、耳环等并不属于医疗器械。
其中,也并未要求检查说明书中是否包含自测/自用等相关字样。
在2022年,NMPA发布的《医疗器械经营监督管理办法》中就明确,“医疗器械零售,是指将医疗器械直接销售给消费者个人使用的医疗器械经营行为”。
而在该办法当中,对医疗器械零售业务的要求和医疗器械批发业务的要求,是完全一致的。
因此,我们可以得出结论,对于直接销售给消费者的医疗器械,只要消费者能够个人自行使用就可以了,而不是必须在说明书当中包含自测/自用等相关字样。
这也就是说,对于IVD试剂来说,只要消费者能够自行采样——例如口腔黏膜、指尖血、尿液、粪便样本等——基本就可以直接销售给消费者使用。
但对于那些需要采集静脉血甚至动脉血样本的检测而言,由于必须要有人帮助采样,所以应该是没有办法直接销售的。
当然,这也不是绝对的,比如,可以提供护士上门采样服务来解决这个问题。看一看京东IVD板块
朋友说,听你分析的,是很有道理,但有没有实际的例子能让我看看,否则我还是放心不下。
当然有,让我们看看京东。
在京东医疗保健板块下面,有一个分支——体外检测试纸/试剂,如果我们将其按照销量排序,那么结果就如下图所示,

可以看到,在销量前十名的产品当中,有四个是新冠抗原、四个是早早孕试剂,另外两个则是艾滋检测试剂。
在国家局网站上,对目前销量排名第一的万孚新冠抗原检测试剂进行查询,结果如下所示,
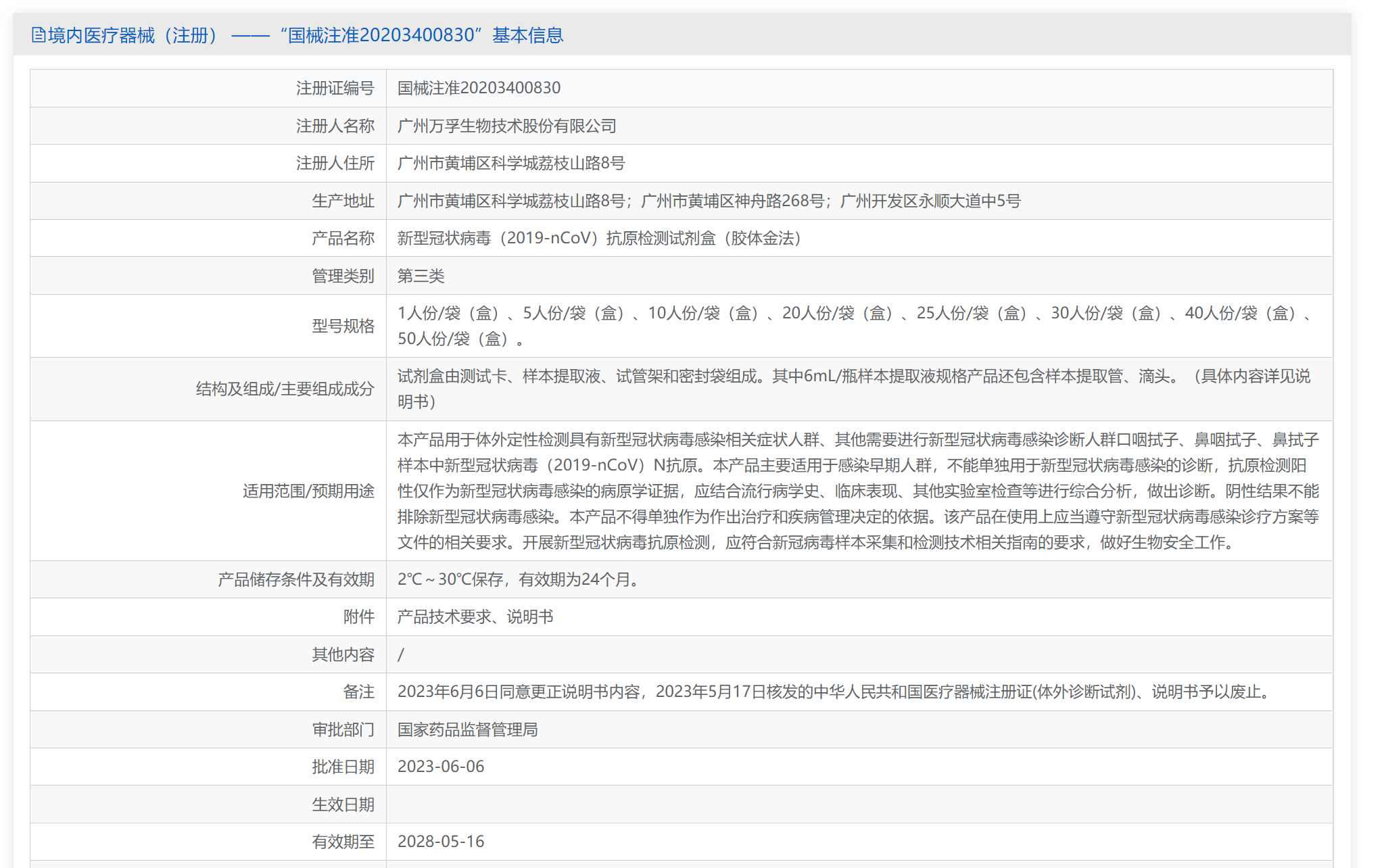
和我们之前的推论相符。
在2022年,诺辉曾宣布其旗下幽门螺杆菌检测产品获得NMPA批准,是NMPA批准的中国首个适用于“消费者自测”的幽门螺杆菌检测产品。
那京东上面,是否只销售诺辉出品的幽门螺杆菌检测产品呢?在京东上,我们以“幽门螺杆菌检测”为关键词进行搜索,搜索结果如下,
可以看到,当前综合排名第一的为天津中新科炬生产的幽门螺旋杆菌(HP)抗原检测试剂盒(胶体金法)(国械注准20173401236),其首次获批时间为2017年,在药监官网查询其相关信息如下所示,
而且,在综合排名前十的产品当中,也并未发现诺辉公司的幽幽管。
所以,在当下,那些消费者能够自行使用产品,正在直接销售给消费者。
对于居家自测产品来说,也是这样,对于大部分IVD厂家来说,是一个全新的未知市场,从To B改为了To C,从面对少数的专业人士,到直面大量的消费者。
在这种情况下,企业会遇到什么样的问题,有没有解决问题的能力,都是未知数。
这个时候,总调研,是没有用的,因为那都是别人的看法。
就好比小马过河,松鼠觉得水深会淹死,老牛觉得水浅完全没问题,这是两者之间的体型差距导致的。
而这水,对于想要进入居家自测市场的IVD厂家来说,是深还是浅呢?
不知道,只能试一试。
在商业上,有一个MVP原则,也就是最小可行产品原则,它的核心理念是在最短的时间内,用最少的资源,构建出一个能够满足目标市场核心需求的产品原型
因此,如果已有产品,就能够直接在市场上进行销售,那就再好不过。
这样做,可以带来两个好处。
第一个,就是产品本身的研发费用已经分摊完毕了,就算试水失败,损失也不会太大。
第二个,也是更重要的一个点,就是能更好的定位问题。
试水的目标,就是为了去发现存在什么样的问题,如果专门设计一个全新的产品,公司内部对这个新产品也没完全吃透,在这种情况下,就很难区分问题出在哪。
是产品设计有问题,还是销售渠道有问题,还是售后服务有问题?
如果没法定位问题,那就很难正确的改进问题,更大可能性是越改越差,最后一地鸡毛。
拿老产品去居家自测市场上试试水吧。
关注我,降低产品上市认知门槛。
*个人观点,仅供参考。